A Mahjong nagyon népszerű szemgimnasztikai elfoglaltság. A kémia szerelmesei számára (akik e hazában nem tudnának tömegdemonstrációt szimpátiatüntetést gyanánt a vegytan mellett :-)) egy kedves, online játékot ajánlok.

Az ingyenes kémiai mahjong-játék a http://www2.stetson.edu/mahjongchem/ címen érhető el a Stetson Unversity jóvoltából.
Az alakzatok között a Turtle (teknős) leginkább hasonlít a szokványos játékhoz. A feladatok közül választhatunk az oxidációs számmal kapcsolatos téglákat, vagy gyakorolhatjuk a bonyolultabb ionok angol elnevezését is. A kedvencem a vegyértékhéjjal kapcsolatos leosztás. A kémiai elemek elektronjai ugyanis nagyon sok szempontból egyenrangúak, de karrierlehetőségeik mégsem egyformák. A nagybetűs élet igazából azoknak az elektronoknak nyílik meg, amelyek olyan energiájúak, hogy egy kémiai barátkozás (kötés) során reflektorfénybe kerülnek. A vegyértékelektronok kapnak társat vagy költöznek át egy másik atom háztartásába (ionos kötés). A vegyértékelektronok közül kerülnek ki a kovalens kötések szereplői is.
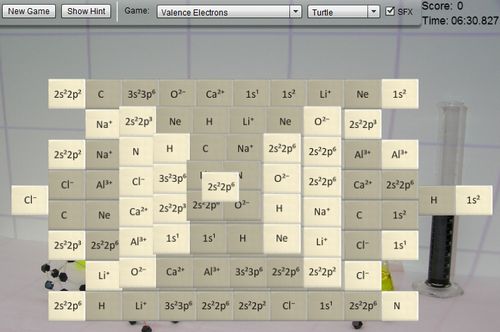
Vegyértékelektronjai (a játékban: Valence electrons) minden elemnek vannak, de vannak olyan, amelyek kevésbé engedik őket bulizni (pl. a nemesgázok) és vannak igazán nagy vegyülős elemek is (pl. a halogének). A játékban atomokat, ionokat és a hozzájuk tartozó vegyértékelektronok jelöléseit kell megtalálni. Itt most 5 perc ijedelem jön, de utána végtelen nyugalom. Aki ijedős, innen már ne olvasson tovább, hanem kattintson ide.
Ezt a játékot akkor élvezhetjük igazán, ha egy periódusos rendszerre kacsintgatunk közben. Az s és a p energiaszinteket jelent. A 2s22p6 azt jelenti, hogy a 2. héjon (ez a periódusos rendszerben a soroknak felel meg) 2+6=8 elektron van (ez a periódusos rendszerben a főcsoportokat adja meg). Vagyis a 2s22p6 párja a neon (Ne), amely a 2. periódusban (sor), a VIII.a jelzésű főcsoportban (oszlop) található.
Ionok esetén viccesebb a dolog, mivel azoknál hozzá kell adni vagy le kell vonni annyi elektront, amennyi a töltésük. Például a Cl- azt jelenti, hogy a klóratom beszerzett egy elektront a meglevő 7 mellé. Miért 7? Mert a VII.a főcsoportban lakik. Ráadásul a 3. periódusban, ezért olyan párt kell neki keresnünk, ahol az s és a p mellett 3-as van és összesen 7+1=8 elektron. A 3s23p6 pont megfelel.
A játék kifejezetten az egyszerű esetekkel szórakoztat, hiszen csak s és p van. Az s szinten maximum 2 elektron lehet, a p szinten pedig 6. A kémiaórák legnyugisabb szereplői vannak a játékban, hiszen nincsenek átmeneti fémek (nekik d szintjük is van) vagy még ravaszabb f mezős fémek.
Aki megunja a kémiai játékot, igazi mahjongot is kérhet, de aki virtuóz, az vizes oldatban csapadékot adó párokat is kereshet. Egy jó kémiakönyvet nem helyettesít ez a játék, de a kémia lovagjai és lovaglányai jól járnak vele.
Ez a helyzet.







Hozzászólások